এ H-S-H বন্ধন কোণের মান কত?
এ H-S-H বন্ধন কোণের মান কত?
Created: 3 years ago |
Updated: 9 months ago
Updated: 9 months ago
-
ক
-
খ
-
গ
-
ঘ
উত্তরঃ
কেন্দ্রীয় পরমাণুর তড়িৎ ঋণাত্মকতা বেশি হলে বন্ধন ইলেকট্রন যুগল কেন্দ্রীয় পরমাণুর দিকে সরে আসে। ফলে বন্ধন কোণের মান বৃদ্ধি পায়। যেমন- H2O ও H2S এর কেন্দ্রীয় পরমাণুর তড়িৎ ঋণাত্মকতা O>S বলে H-O-H বন্ধন কোণ 104.5° ও H-S-H বন্ধন কোণ 92.1° হয়।
Jhorna
3 years ago

MD.SOLAIMAN HOSAN
2 years ago
| যৌগ অণু | অরবিটাল সংকরণ | বন্ধন ইলেকট্রন জোড় | নিঃসঙ্গ ইলেকট্রন জোড় | তড়িৎ ঋণাত্মকতা | বন্ধন কোণ | অণুর গঠন আকৃতি |
৩ জোড়া ৩ জোড়া | ১ জোড়া ১ জোড়া | 3.0-2.1 3.0-4.0 | ত্রিকোণাকার পিরামিড ত্রিকোণাকার পিরামিড | |||
৩ জোড়া ৩ জোড়া | ১ জোড়া ১ জোড়া | 3.0-2.1 2.1-2.1 | ত্রিকোণাকার পিরামিড ত্রিকোণাকার পিরামিড | |||
২ জোড়া ২ জোড়া | ২ জোড়া ২ জোড়া | 3.5-2.1 2.5-2.1 | বিকৃত চতুস্তলকের V আকৃতি বিকৃত চতুস্তলকের V আকৃতি |
Shakib Al Hasan
3 years ago
Related Question
View All
Created: 3 years ago |
Updated: 4 months ago
Updated: 4 months ago
-
ক
আয়নিক ও সমযোজী
-
খ
আয়নিক ও ভ্যানডার ওয়ালস সমযোজী
-
গ
সমযোজী ও হাইড্রোজেন
-
ঘ
হাইড্রোজেন ও সন্নিবেশ
Created: 3 years ago |
Updated: 6 months ago
Updated: 6 months ago
-
ক
ধাতব
-
খ
আয়নিক
-
গ
সন্নিবেশ
-
ঘ
সমযোজী
Created: 3 years ago |
Updated: 5 months ago
Updated: 5 months ago
-
ক
-
খ
-
গ
-
ঘ
Created: 3 years ago |
Updated: 6 months ago
Updated: 6 months ago
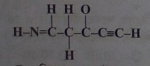
-
ক
8 সিগমা ও 7 পাই
-
খ
8 সিগমা ও 3 পাই
-
গ
11 সিগমা ও 3 পাই
-
ঘ
11 সিগমা ও 4 পাই
শিক্ষকদের জন্য বিশেষভাবে তৈরি
১ ক্লিকে প্রশ্ন, শীট, সাজেশন ও
অনলাইন পরীক্ষা তৈরির সফটওয়্যার!
শুধু প্রশ্ন সিলেক্ট করুন — প্রশ্নপত্র অটোমেটিক তৈরি!
প্রশ্ন এডিট করা যাবে
জলছাপ দেয়া যাবে
ঠিকানা যুক্ত করা যাবে
Logo, Motto যুক্ত হবে
অটো প্রতিষ্ঠানের নাম
অটো সময়, পূর্ণমান
প্রশ্ন এডিট করা যাবে
জলছাপ দেয়া যাবে
ঠিকানা যুক্ত করা যাবে
Logo, Motto যুক্ত হবে
অটো প্রতিষ্ঠানের নাম
অটো সময়, পূর্ণমান
অটো নির্দেশনা (এডিটযোগ্য)
অটো বিষয় ও অধ্যায়
OMR সংযুক্ত করা যাবে
ফন্ট, কলাম, ডিভাইডার
প্রশ্ন/অপশন স্টাইল পরিবর্তন
সেট কোড, বিষয় কোড
অটো নির্দেশনা (এডিটযোগ্য)
অটো বিষয় ও অধ্যায়
OMR সংযুক্ত করা যাবে
ফন্ট, কলাম, ডিভাইডার
প্রশ্ন/অপশন স্টাইল পরিবর্তন
সেট কোড, বিষয় কোড
Related Question
মাত্র ১৫ পয়সায় প্রশ্নপত্র
১ ক্লিকে প্রশ্ন, শীট, সাজেশন তৈরি করুন আজই
Question Analytics
মোট উত্তরদাতা
জন
সঠিক
ভুল
উত্তর নেই


